
Лечение инфекций мочевыводящих путей препаратом Канефрон® в Германии: ретроспективный анализ базы данных
Martina Höller1 , Hubert Steindl1, Dimitri Abramov-Sommariva1, Florian Wagenlehner2 , Kurt G. Naber3 та Karel Kostev4,*
- Компания «Бионорика СЭ», Кершенштайнерштрассе 11–15, 92318 Ноймаркт, Германия (Kerschensteinerstrasse 11–15, 92318 Neumarkt, Germany); Martina.Hoeller@bionorica.de (MH); Хуберт. Steindl@bionorica.de (H.S.); Dimitri.Abramov-Sommariva@bionorica.de (D.A.-S.)
- Клиника урологии, детской урологии и андрологии, Гиссенский университет им. Юстуса-Либиха, Рудольф-Бухгайм-Штрассе 7, 35392 г. Гиссен, Германия (Rudolf-Buchheim-Straße 7, 35392 Giessen, Germany); wagenlehner@aol.com
- Кафедра урологии, Мюнхенский технический университет, PA: Карл-Бикледер-Штрассе 44c, 94315 г. Штраубинг, Германия (Karl-Bickleder Street 44c, 94315 Straubing, Germany); kurt@nabers.de
- Отдел эпидемиологии компании IQVIA, Унтершвайнстиге 2-14, 60549, г. Франкфурт-на-Майне, Германия (Unterschweinstiege 2-14, 60549 IQVIA, Frankfurt Am Main, Germany)
* Адрес для переписки: karel.kostev@iqvia.com
Аннотация:
Цель: Целью данного исследования было провести оценку лечения препаратом Канефрон после установления диагноза острого цистита или инфекции мочевыводящих путей (ИСШ) относительно риска спорадических рецидивных ИСШ, частых рецидивных ИСШ; продолжительности временной нетрудоспособности, обусловленной ИСШ; дополнительное назначение антибиотиков и осложнений со стороны почек (пиелонефрита) по сравнению со стандартной антибиотикотерапией.
Методы: Это ретроспективное когортное исследование основывалось на информации из базы данных «Анализатор заболеваний IMS®» (IMS® Disease Analyzer, собственность компании «IQVIA»). В анализ были включены амбулаторные пациенты в Германии, которым по крайней мере один раз был поставлен диагноз острого цистита или ИСШ и назначен Канефрон® или стандартная антибиотикотерапия в период с января 2016 г. по июнь 2019 г. врачом общей практики (ЛЗП), гин и в них были получены соответствующие данные. Для изучения взаимосвязей между назначением препарата Канефрон и количеством спорадических или частых рецидивных ИСШ, а также длительностью временной нетрудоспособности, обусловленной ИСШ, количеством дополнительных назначений антибиотиков и количеством случаев пиелонефрита использовались модели многопараметрической регрессии. Для эффектов препарата Канефрон® была использована поправка на возраст, пол, страховой статус и индекс коморбидности Чарльсона (Charlson Comorbidity Score, ИКЧ). Результаты: Для проведения анализа были доступны данные о 2320 пациентах, получавших Канефрон и 158 592 пациентов, получавших антибиотики. По сравнению с назначением антибиотиков, назначение Канефрона® было значительно связано с уменьшением частоты спорадических рецидивов ИСШ в течение 30–365 дней после индексной даты (соотношение шансов (СШ): 0,66; 95%, доверительный интервал (ДИ): 0,58 ‒0,72), а также с уменьшением частоты рецидивов ИСШ (СШ: 0,61; 95% ДИ: 0,49‒0,88), и с небольшой частотой дополнительного назначения антибиотиков в течение 31–365 дней (СШ: 0, 57; 95 % ДИ: 0,52–0,63). Между когортами пациентов, получавших Канефрон и антибиотикотерапию, не наблюдалось значимых отличий относительно вероятности того, что пациент возьмет больничный (СШ: 0,99; 95% ДИ: 0,86-1,14), вероятности нового назначения антибиотиков в течение 1- 30 дней (СШ: 1,01; 95% ДИ: 0,87-1,16) и частоты возникновения пиелонефрита (соотношение шансов (СШ): 1,00; 95% ДИ: 0,67-1,48).
Вывод: Вышеприведенные данные из реальной практики указывают на то, что Канефрон® — эффективное и безопасное средство симптоматической терапии острого цистита или ИСШ. Его следует рассматривать в качестве альтернативного средства лечения; в частности, учитывая необходимость более широкого внедрения стратегии рационального использования противомикробных препаратов.
Ключевые слова:
- Канефрон;
- антибиотики;
- инфекции мочевыводящих путей;
- когортное исследование;
- фитотерапия.
1. Введение
Во всем мире инфекции мочевыводящих путей (ИСШ) поражают около 150 миллионов человек ежегодно 1 и являются одной из ведущих причин обращения взрослого населения за первичной медицинской помощью 2. По данным Foxman, почти у половины всех женщин в течение жизни возникает по крайней мере один эпизод цистита, а около трети женщин имеет по крайней мере один эпизод цистита к 24-летнему возрасту 3. В большинстве случаев ИСШ — это острый неосложненный цистит 4, а действующие наставления в качестве терапии первой линии рекомендуют применять антибиотики 5,6.
В качестве ответа на стремительный рост количества резистентных штаммов бактерий принципы рационального использования антибиотиков призывают осмотрительно применить антибиотики там, где это необходимо, и воздерживаться от применения антибиотиков, если это возможно. В большинстве случаев неосложненных инфекций иммунная система организма способна справиться с патогенными бактериями; таким образом, антибиотики не являются безоговорочно показанными 7. Соответственно, «Руководства ЕС по осторожному применению противомикробных препаратов в медицине» (2017) в целом рекомендуют врачам избегать назначения антибактериальных препаратов, когда имеющиеся данные свидетельствуют о наличии только вирусной инфекции или самоограничивающей бактериальной инфекции. Исходя из этой необходимости (избегать назначения антибиотиков там, где это возможно), средства симптоматической терапии, не являющиеся антибиотиками, заняли важное место в лечении пациентов с неосложненными ИМП. До этого времени в исследованиях проводилось сравнение эффективности нестероидных противовоспалительных препаратов (НПВП), например, ибупрофена 8,9 или диклофенака 10 и антибиотиков. Поскольку данные этих исследований указывают на достаточно высокую эффективность такого лечения, на сегодняшний день несколько инструкций также рекомендуют назначать средства, не являющиеся антибиотиками. Согласно действующим установкам Европейской ассоциации урологов (EAU) 5, а также немецких междисциплинарных установок AWMF S3 6, антибиотики все еще считаются вариантом терапии первой линии при ИСШ, но в случаях острого неосложненного цистита с легко или умеренно выраженными симптомами следует рассмотреть возможность назначения средств симптоматической терапии, не являющихся антибиотиками. Назначение лекарственных средств растительного происхождения также считается подобающим подходом к лечению ИСШ «без антибиотиков» 11,12. Одним из таких средств, утвержденным для использования в 31 стране, является Канефрон®, в состав которого входят трава золототысячника (Centaurium erythraea Rafn, herba), корень любистка (Levisticum officinale Koch, radix) и листья розмарина (Rosmarinus officinalis Linné, folium) 13. Канефрон ® проявляет так называемые «многоцелевые» свойства, в том числе оказывает спазмолитическое 14, мочегонное 15, антиоксидантное 16, антиадгезивное 17, противовоспалительное и обезболивающее 18 действие.
Эффективность Канефрона® была продемонстрирована в целом ряде клинических исследований 13,19-21.
Недавно Wagenlehner et al. в рандомизированном двойно слепом исследовании фазы III показали, что эффективность Канефрона при лечении острых НИСШ в нижних отделах мочевыводящих путей у женщин не уступает антибиотикотерапии (фосфомицина трометамол) по показателю «предупреждения дополнительного применения антибиотиков для показания .
По мнению Haynes, оценка соотношения «польза-риск» для лекарственных средств должна проводиться не только в условиях исследования (т.е. отвечать на вопрос «способен ли этот препарат «работать»?»), но и подтверждаться в реальных условиях («работает»). этот препарат?», «стоит ли его применять?») 22. Поэтому целью данного исследования было доказать, основываясь на данных из реальной клинической практики, эффективность монотерапии препаратом Канефрон в качестве средства симптоматической терапии ИСШ при обычных условиях клинической практики и подтвердить таким образом клинические данные, полученные в ранее проведенных интервенционных исследованиях. Таким образом, мы провели оценку частоты назначений Канефрона (в виде препарата Канефрон Н или препарата Канефрон УНО) в качестве лечения после установления диагноза острого цистита или ИСШ, а также потребности в дополнительном назначении антибиотиков по сравнению со стандартной антибиотикотерапией. Поскольку риск рецидива заболевания, его осложнений, а также продолжительность заболевания являются частыми причинами назначения антибиотиков, мы также исследовали влияние монотерапии препаратом Канефрон на спорадические и частые рецидивирующие ИСШ, пиелонефрит и продолжительность временной нетрудоспособности, обусловленной ИСШ.
2. Материалы и методы
2.1. Источники данных
Этот анализ основывался на информации из базы данных «Анализатор заболеваний IMS®», в которой содержатся сведения о клинических случаях, предоставленные врачами амбулаторий (как врачами общей практики ЛПЗ, так и врачами-специалистами) в Германии. В этой базе данных содержится информация о демографических данных пациентов, назначениях лекарственных препаратов, сопутствующих лекарственных средств, сопутствующих заболеваний, временной нетрудоспособности и направлений в стационарные медицинские учреждения. При проведении анализа данных мы учитывали данные только из тех медицинских учреждений, которые ранее регулярно направляли сведения в экспертную группу IMS®DA. IMS®DA содержит данные о более чем 10 миллионах пациентов, внесенные в промежутке между 2015 и 2019 годами.
Информацию предоставляют около 3000 врачей амбулаторий, представляющих около 3% всех амбулаторий и частных практик в Германии. Выборка амбулаторий/частных практик, включенная в исследование, является географически репрезентативной для Германии и охватывает восемь основных регионов страны. Примененные в Германии методы формирования выборки для отбора амбулаторий/частных практик врачей являются надлежащими и обеспечивают получение репрезентативной базы данных амбулаторий общей практики и специализированных амбулаторий 23.
Законодательство Германии при определенных условиях разрешает использование в исследовательских целях анонимных данных электронной медицинской документации. Согласно этому законодательству, для проведения такого типа обсервационного исследования, не предусматривающего использование данных, которые могли бы непосредственно идентифицировать пациента, нет необходимости получать информированное согласие от пациентов или разрешение соответствующего экспертного совета учреждения здравоохранения (ЭРЖ). Поскольку данные о пациентах спрашивали только в совокупном виде и в ответ на такие запросы не предоставлялось никакой конфиденциальной медицинской информации, для использования этой базы данных и для проведения данного исследования не требовалось никаких разрешений от ЭРЖ.
2.2. Выборка исследования и переменные
В это ретроспективное когортное исследование включены пациенты с по крайней мере одним диагнозом острого цистита (МКБ-10: N30.0) или ИСШ (МКБ-10: N39.0), установленным в период между 01 января 2016 г. и 30 июня 2019 г. одной из амбулаторий ЛОП, гинеколога или уролога, из которых были получены данные. Дата первого диагноза, документированного в течение этого периода, считалась индексной датой. К другим критериям включения относилось по крайней мере 12 месяцев наблюдения перед установлением этого диагноза, что подтверждалось записью о по крайней мере один визит к врачу в течение периода в ≥365 дней до индексной даты, а также назначения Канефрона Н или Канефрона УНО или стандартного антибиотика (код ATX: J01) в индексную дату. Пациенты, которым был назначен антибиотик в течение 30 дней до индексной даты; пациенты, которым назначались другие фитопрепараты в течение периода исследования, и пациенты, которым в индексную дату был назначен Канефрон вместе с любым антибиотиком, не допускались к участию в исследовании. Пациенты были распределены на две когорты: когорта препарата Канефрон и когорта антибиотикотерапии; обе когорты впоследствии сравнивались друг с другом.
К переменным, которые использовались в данном исследовании, относились возраст, пол, покрытие медицинским страхованием (частным или обязательным общегосударственным), специальность врача (ЛЗП, гинеколог, уролог) и индекс коморбидности Чарльсона (ИКЧ). ИКЧ — это метод категоризации имеющихся у пациента сопутствующих заболеваний, основанный на Международной классификации болезней (МКБ) и содержащий 19 категорий. Чем выше балл, тем с большей вероятностью предусмотренный результат приведет к смерти или более интенсивному использованию ресурсов здравоохранения 24.
2.3. Статистические анализы
Определялись отличия относительно доли пациентов: (1) с спорадическими рецидивами ИСШ, которые определялись как наличие по меньшей мере одного заново подтвержденного диагноза ИСШ (МКБ-10: N39.0) или острого цистита (МКБ-10: N30.0) в течение 30-365 дней с момента установления первоначального диагноза; (2) с частыми рецидивирующими ИСШ, определяемыми по руководящим установкам EAU 5 как минимум три диагноза инфекций мочевыводящих путей в течение 2–365 дней с момента установления первичного диагноза или по крайней мере два диагноза инфекции мочевыводящих путей в течение 2–184 дней установление первичного диагноза; (3) с временной нетрудоспособностью, определяемой ИПШ, которая определяется как документально подтвержденная временная нетрудоспособность в течение одного месяца после установления диагноза ИСШ; (4) которым по крайней мере один раз были назначены антибиотики в течение 1–30 дней после установления диагноза или позже (30–365 дней); и (5) с наличием исходного документально подтвержденного диагноза пиелонефрита (МКБ-10: N10-12) в течение срока продолжительностью до 3 лет после установления диагноза ИСШ.
Для изучения взаимосвязей между назначением Канефрона и уменьшением риска спорадических рецидивов ИСШ или частых рецидивных ИСШ, длительностью временной нетрудоспособности, обусловленной ИСШ, и назначением антибиотиков, использовались модели многопараметрической логистической регрессии. Для эффектов препарата Канефрон® была использована поправка на возраст, пол, страховой статус и ИКК. Модели многопараметрической регрессии также строились отдельно для лиц мужского и женского пола и трех возрастных групп (≤40, 41–60, >60 лет). Критерием статистической значимости считалось р-значение <0,05.
Расчет различий между когортой препарата Канефрон и когортой антибиотикотерапии относительно процентных долей пациентов, у которых было первоначально задокументировано возникновение пиелонефрита в течение срока продолжительностью до 3 лет после установления диагноза ИСШ, проводился по методу Каплана-Мейера. Данные относительно пациентов с задокументированным диагнозом пиелонефрита, возникшего до индексной даты, были изъяты из данного анализа. Для изучения взаимосвязи между назначением Канефрона и вероятностью возникновения пиелонефрита (с поправкой на возраст, пол, страховой статус и ИКК) использовалась модель многопараметрической регрессии Кокса.
3. Результаты
3.1. Отбор пациентов и характеристики на исходном уровне у пациентов, принявших участие в исследовании
Из 232875 пациентов, которым был установлен диагноз ИСШ (МКБ-10: N39.0) или острого цистита (МКБ 10: N30.0), и наблюдавшихся в течение не менее 365 дней до индексной даты, в день установления диагноза Канефрон® Н или Канефрон УНО было назначено 3343 (1,40%) пациентам, а антибиотики — 160082 (68,74%) пациентам. После исключения пациентов, у которых Канефрон сочетался с антибиотиками, и пациентов, получавших другие фитопрепараты для лечения ИСШ, а также после исключения пациентов, принимавших другие препараты для лечения ИСШ (например, препараты, содержащие маннозу, метионин или арбутин) с когорты Канефрона®, в целом были доступны для анализа данные о 2320 пациентах, получавших Канефрон®, и 158 592 пациентов, получавших антибиотики (Рисунок 1).
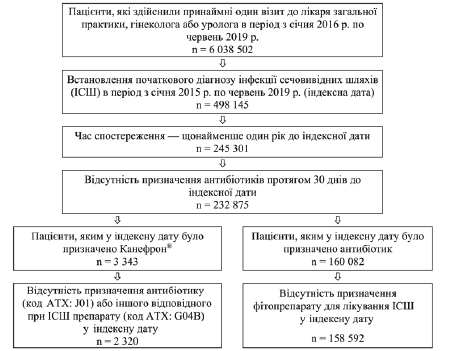
Рисунок 1. Отбор пациентов для участия в исследовании.
Из 69 450 пациентов, не включенных в анализ из-за того, что им в индексную дату не был назначен ни Канефрон, ни антибиотик, у 93% не было назначено ни одного препарата по поводу ИСШ или острого цистита. При этом только 7% получили какое-то назначение (3% анальгетик, 3% препараты, содержащие арбутин, и менее 1% другие препараты).
В общей сложности у 4% пациентов в когорте Канефрона® был параллельно назначен анальгетик, в то время как в когорте антибиотикотерапии ~3% пациентов получали анальгетики и только у 1% были назначены другие препараты (например, препараты, содержащие маннозу, метионин или арбутин) .
В таблице 1 приведены характеристики принявших участие в исследовании пациентов на исходном уровне. Пациенты, принимавшие Канефрон, были значительно моложе (51,3 (СВ: 19,9) по сравнению с 55,0 (СВ: 20,8) лет) и имели несколько более низкий индекс коморбидности (1,6 по сравнению с 1 ,7), чем пациенты, которым были назначены антибиотики. Процентная доля пациентов женского пола (81,2% по сравнению с 90,8%) была значительно ниже, а процентная доля пациентов с частной медицинской страховкой (11,3% по сравнению с 7,6%) была значительно выше среди пациентов, что получали Канефрон, чем среди пациентов в когорте антибиотикотерапии. Большинство пациентов в обоих когортах лечились в ЛОП (90,0% по сравнению с 80,7%). Имеющиеся отличия относительно характеристик на исходном уровне указывали на необходимость проведения анализов со стратификацией по показателям «возраст» и «пол».
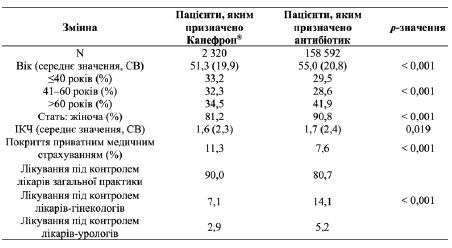
Таблица 1. Основные характеристики пациентов, участвовавших в исследовании
3.2. Спорадические рецидивирующие инфекции мочевыводящих путей
В течение 30–365 дней после индексной даты у 12,3% пациентов, которым был назначен Канефрон, и у 17,2% пациентов, которым были назначены антибиотики, был задокументирован по крайней мере один заново подтвержденный диагноз ИПШ. Назначение Канефрона ассоциировалось со значительно ниже шансами на по крайней мере один заново подтвержденный диагноз ИСШ в течение 30-365 дней после индексной даты (соотношение шансов (СШ): 0,66; 95% доверительный интервал (ДИ): 0,52‒ p<0,001). Эта взаимосвязь наблюдалась у лиц мужского и женского пола, а также в разных возрастных группах (рисунок 2).
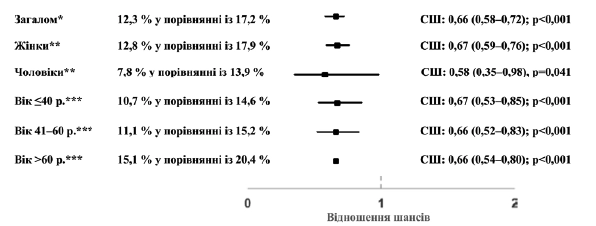
Рисунок 2. Взаимосвязь между назначением Канефрона® и наличием нового подтвержденного диагноза спорадической ИСШ в течение 30–365 дней после индексной даты (Канефрон® по сравнению с антибиотиком). Многопараметрическая логистическая регрессия с поправкой на возраст и пол пациента, покрытие медицинским страхованием, специальность врача амбулатории и ИКЧ. Многопараметрическая логистическая регрессия с поправкой на возраст пациента, покрытие медицинским страхованием, специальность врача амбулатории и ИКЧ. ***Многопараметрическая логистическая регрессия с поправкой на пол пациента, покрытие медицинским страхованием, специальность врача амбулатории и ИКЧ.
3.3. Частые рецидивирующие инфекции мочевыводящих путей
Наличие по крайней мере трех диагнозов ИСШ, установленных в течение 2–365 дней с момента установления первичного диагноза, или наличие по крайней мере двух диагнозов ИСШ, установленных в течение 2–184 дней с момента установления первичного диагноза, было задокументировано у 3,1% пациентов, которым был назначен Канефрон ® и у 5,0% пациентов, которым были назначены антибиотики. Назначение Канефрона ассоциировалось со значительно более низкими шансами появления частых рецидивных ИСШ (СШ: 0,601; 95% ДИ: 0,49–0,88; p < 0,001). Эта взаимосвязь (значимая или в виде тенденции) наблюдалась у лиц мужского и женского пола и во всех возрастных группах (рисунок 3).
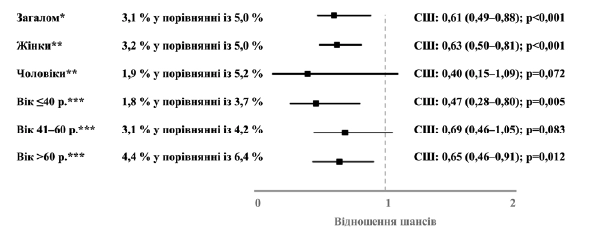
Рисунок 3. Взаимосвязь между назначением Канефрона® и вероятностью возникновения частых рецидивных ИСШ (Канефрон® по сравнению с антибиотиком). Многопараметрическая логистическая регрессия с поправкой на возраст и пол пациента, покрытие медицинским страхованием, специальность врача амбулатории и ИКЧ. Многопараметрическая логистическая регрессия с поправкой на возраст пациента, покрытие медицинским страхованием, специальность врача амбулатории и ИКЧ. *** Многопараметрическая логистическая регрессия с поправкой на пол пациента, покрытие медицинским страхованием, специальность врача амбулатории и ИКК.
3.4. Продолжительность временной нетрудоспособности в связи с инфекцией мочевыводящих путей
Всего 16,9% пациентов, которым был назначен Канефрон, и 18,2% пациентов, которым были назначены антибиотики, приняли по меньшей мере 3 дня больничного в связи с ИСШ. Не наблюдалось значимой взаимосвязи между назначением Канефрона и шансами на то, что пациент возьмет больничный (СШ: 0,99; 95% ДИ: 0,86–1,14; p = 0,931); кроме того, никакой такой взаимосвязи не наблюдалось в проанализированных подгруппах (рисунок
4). В качестве анализа чувствительности проводилось изучение взаимосвязи между назначением Канефрона и вероятностью того, что пациент возьмет больничный по меньшей мере на 7, 10 или 14 дней. Не наблюдалось никаких значимых взаимосвязей в моделях многопараметрической регрессии; не было найдено никаких отличий между когортами
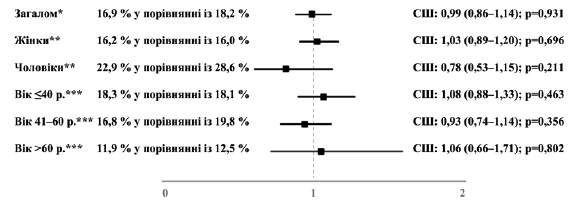
Рисунок 4. Взаимосвязь между назначением Канефрона® и вероятностью того, что пациент возьмет больничный продолжительностью не менее 3 дней (Канефрон® по сравнению с антибиотиком). Многопараметрическая логистическая регрессия с поправкой на возраст и пол пациента, покрытие медицинским страхованием, специальность врача амбулатории и ИКЧ. Многопараметрическая логистическая регрессия с поправкой на возраст пациента, покрытие медицинским страхованием, специальность врача амбулатории и ИКЧ. *** Многопараметрическая логистическая регрессия с поправкой на пол пациента, покрытие медицинским страхованием, специальность врача амбулатории и ИКЧ
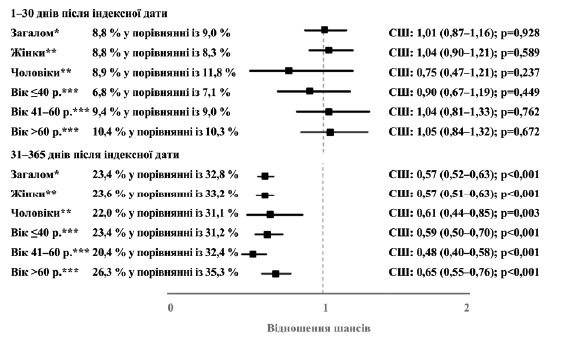
Рисунок 5. Взаимосвязь между назначением Канефрона® и вероятностью назначения антибиотика в период 31–365 дней или 1–30 дней после индексной даты (Канефрон® по сравнению с антибиотиком). Многопараметрическая логистическая регрессия с поправкой на возраст и пол пациента, покрытие медицинским страхованием, специальность врача амбулатории и ИКЧ. Многопараметрическая логистическая регрессия с поправкой на возраст пациента, покрытие медицинским страхованием, специальность врача амбулатории и ИКЧ. *** Многопараметрическая логистическая регрессия с поправкой на пол пациента, покрытие медицинским страхованием, специальность врача амбулатории и ИКК.
Канефрона® и антибиотикотерапии (СШ: 1,01 (95% ДИ: 0,85‒1,19; p = 0,949) для срока ≥7 дней: СШ: 1,04 (95% ДИ: 0,86‒1,25) ;p = 0,703) для срока ≥10 дней, СШ: 1,06 (95% ДИ: 0,86‒1,31; p = 0,584) для срока ≥14 дней.
3.5. Дополнительное назначение антибиотиков после индексной даты
В течение 31-365 дней после индексной даты у 23,4% пациентов, которым был назначен Канефрон, и у 32,8% пациентов, которым были назначены антибиотики, имело место по крайней мере одно новое (повторное) назначение антибиотиков. Назначение Канефрона ассоциировалось со значительно более низкими шансами назначения антибиотиков в течение 31–365 дней после индексной даты (СШ: 0,57; 95% ДИ: 0,52–0,63; p<0,001). Эта взаимосвязь наблюдалась во всех исследуемых подгруппах (рисунок 5). При этом, однако, не наблюдалось никакой взаимосвязи между назначением Канефрона и назначением антибиотиков в срок 1–30 дней после индексной даты (СШ: 1,01; 95 % ДИ: 0,87–1,16; p=0,921) .
3.6. Частота возникновения пиелонефрита
В течение срока до 3 лет после индексной даты пиелонефрит возникал относительно редко. Наличие пиелонефрита в начале было документировано у 1,6% пациентов из группы Канефрона и у 1,5% пациентов из группы антибиотикотерапии; по данным анализа на основании многопараметрической регрессии Кокса, никакой значимой взаимосвязи не наблюдалось (соотношение шансов (СШ): 1,00; 95% ДИ: 0,67–1,48; p=0,954).
4. Обсуждение
Насколько нам известно, это первое неинтервенционное исследование в реальных условиях, проведенное в Германии, доказывающее, что монотерапия препаратом Канефрон на самом деле «работает» в качестве симптоматического лечения ИСШ. Полученные данные подтверждают важную роль, которую препарат Канефрон играет в уменьшении применения антибиотиков и ослаблении антибиотикорезистентности.
Представленные результаты не являются чем-то неожиданным, поскольку Канефрон® - это хорошо исследованный и утвержденный лекарственный препарат. Amdii et al. ранее пришли к выводу, что лечение препаратом Канефрон Н позволяет сократить применение антибиотиков у женщин с НИШ 25. Исследовательская группа Wagenlehner et al. провела исследование фазы III для демонстрации не меньшей эффективности, в котором приняло участие 659 женщин. Авторы выявили различие относительно процентной доли женщин, нуждавшихся в дополнительной антибактериальной терапии, между пациентами, получавшими Канефрон Н, и пациентами, получавшими антибиотики; при этом данное отличие свидетельствовало о не меньшей эффективности исследуемого препарата 21. В нашем исследовании анализ по показателю дополнительного назначения антибиотиков проводился для двух временных периодов (1–30 дней и 31–365 дней после установления диагноза ИСШ). В течение 1–30 дней не наблюдалось никаких значимых различий между препаратом Канефрон и антибиотикотерапией. Эти данные подтверждают результаты клинического исследования, проведенного Wagenlehner et al. 21 в реальных условиях. Что касается периода 31–365 дней, частота дополнительного назначения антибиотиков после лечения Канефроном была значительно ниже по сравнению с антибиотикотерапией.
В нескольких клинических исследованиях был описан профилактический эффект препарата Канефрон Н, применявшийся в качестве комбинированной или монотерапии у пациентов, страдающих ИПШ 26-30.
В следующем клиническом исследовании по авторству Davidov и Bunova проводилась сравнительная оценка эффективности и безопасности монотерапии препаратом Канефрон Н и антибиотикотерапии (ципрофлоксацин) при лечении острого цистита легкой степени у 160 женщин 19. Через 6 дней лечения клинические симптомы полностью исчезли у 66 (82,5%) пациентов в группе Канефрона Н и у 68 (85,0%) пациентов в группе антибиотикотерапии. Рецидивы цистита в течение одного года наблюдались у 5% пациентов в группе Канефрона Н и у 12,5% пациентов в группе антибиотикотерапии 19. Интересно отметить, что RWD указывает на то, что у всех пациентов применение Канефрона характеризовалось не только значимо низшим риском спорадического рецидивирования ИСШ, но даже низшим риском возникновения частых рецидивных ИСШ.
Канефрон ® — не только эффективное средство для лечения ИСШ, но и хорошо переносится 31. В отличие от антибиотиков, это лекарственное средство растительного происхождения не оказывает негативного влияния на микробиот кишечника по сравнению с такими препаратами, как фосфомицин или нитрофурантоин 32. Этот эффект становится особенно заметным по мере того, как исследования микробиому мочевыводящих путей показывают, что бессимптомная бактериурия предположительно оказывает защитное действие при ИСШ 33 и может рассматриваться в качестве метода профилактического лечения при рецидивных инфекциях 34. Представленные нами результаты подтверждают этот вывод, поскольку применение антибиотикотерапии ассоциировалось со значительно более высокой вероятностью дальнейшего назначения антибиотиков в период 31-365 дней.
С целью уменьшить количество назначений антибиотиков, в течение последних лет проводилось изучение нескольких лекарственных средств, не являющихся антибиотиками, таких как нестероидные противовоспалительные препараты (НПВП) 8-10 или различные препараты с растительными компонентами, такие как Ангоцин ® ]. По сравнению с НПВП Канефрон® не только обладает обезболивающим/противовоспалительным эффектом, но и оказывает действие различными способами для облегчения симптомов благодаря нескольким компонентам лекарственной смеси (1:1:1), в состав которой входят трава золототысячника, корень любистка и листья розмарина. Благодаря своему спазмолитическому 14, противовоспалительному и обезболивающему 18 действию, Канефрон® имеет потенциал для уменьшения симптомов, связанных с острыми НИСШ в нижних отделах мочевыводящих путей, таких как воспалительная боль, спазм и частое мочеиспускание. Кроме того антиадгезивное действие 17 способствует устранению бактерий из мочевыводящих путей. В нашем ретроспективном исследовании показано, что среди врачей существует определенная степень восприятия средств, не являющихся антибиотиками, поскольку в клинической практике почти треть пациентов (31,3%) не получали антибиотикотерапии. В более чем 2320 из этих случаев проводилось лечение препаратом Канефрон в качестве монотерапии. ЛЗП назначали Канефрон чаще, чем гинекологи или урологи. Это отражает тот факт, что в Германии пациенты, страдающие НИСП, в первую очередь обращаются к ЛЗП.
Пиелонефрит может возникать в качестве осложнения в 0,3% - 0,5% случаев инфекций мочевыводящих путей 8,10. Несмотря на наличие сообщений о высокой частоте возникновения пиелонефрита на фоне применения альтернативных средств, не являющихся антибиотиками 8,10,21, результаты ретроспективного долгосрочного анализа данных дальнейшего наблюдения указывают на то, что не являющиеся антибиотиками средства не оказывают негативного влияния на частоту возникновения пиелонефрита 9. В нашем исследовании также не было выявлено никакой значимой взаимосвязи между применением Канефрона и частотой возникновения пиелонефрита. Кроме того, длительность временной нетрудоспособности, обусловленной ИСШ, при применении препарата Канефрон была такой же, как при применении антибиотикотерапии.
Эти результаты подтверждают гипотезу о том, что симптоматическую терапию препаратом Канефрон следует использовать преимущественно при лечении НИСШ в нижних отделах мочевыводящих путей вместо «априорного» применения антибиотикотерапии.
К сильным сторонам данного исследования относятся большой массив данных (более 2300 пациентов, получавших Канефрон®, и более 158 000 пациентов, получавших антибиотики), включающий пациентов женского и мужского пола, а также различные возрастные группы и специальности врачей. Кроме того, в нашем исследовании использовалась немецкая база данных IMS DA, надежность которой была подтверждена несколькими клиническими исследованиями; следовательно, это свидетельствует о надежности полученных нами результатов 22,35.
Используемая нами база данных IMS®DA обладает определенными особыми характеристиками, которые необходимо принять во внимание. Во-первых, оценки зависят от кодов МКБ, вводимых в систему ЛЗП, врачи-урологи и врачи-гинекологи. Эти коды проходят процесс проверки и подтверждения, осуществляемый владельцем базы данных IMS®DA (компания «IQVIA»). Однако коды МКБ не позволяют провести дифференциацию между осложненными и неосложненными диагнозами. Во-вторых, количество пациентов, получавших лечение Канефроном, было заметно ниже по сравнению с количеством пациентов, лечившихся антибиотиками. Меньшее количество назначений лекарственных средств растительного происхождения может быть обусловлено их регистрационным статусом в Германии, где они являются безрецептурными (OTC) препаратами, в то время как антибиотики рецептурными. Эта база данных не содержит данных об использовании лекарственных средств растительного происхождения, которые пациенты приобрели без рецепта. То же касается НПВП. Возможно, врачи решили не назначать никаких препаратов пациентам с ИСШ очень легкой степени или только предоставляли им рекомендации по безрецептурным препаратам, которые пациенты могли бы впоследствии купить в аптеках самостоятельно. Кроме того, не были доступны данные о социально-экономическом статусе пациентов и факторов риска, обусловленных образом жизни (курение, употребление алкоголя, физическая активность и т.п.). К тому же пациента можно отследить только в единой частной практике/амбулатории; если ему устанавливает диагноз или выписывает лекарство другой врач, такие назначения не документируются.
Чтобы уменьшить вероятность систематической ошибки, в дополнение к поправкам, внесенным в модели регрессии, были отдельно построены модели регрессии для трех возрастов, мужчин и женщин.
В завершение следует отметить, что данное исследование выявило, что в реальных условиях Канефрон уже применяется в качестве монотерапии для лечения ИСШ. Более того, несмотря на свойственные используемой базе данных ограничения, полученные результаты указывают на то, что симптоматическое лечение препаратом Канефрон в качестве монотерапии является эффективным и безопасным. При применении препарата Канефрон частота возникновения спорадических и частых рецидивов ИСШ была даже значительно меньше по сравнению с антибиотикотерапией. Таким образом, симптоматическая терапия неосложненных инфекций нижних отделов мочевыводящих путей растительным лекарственным средством Канефрон рекомендуется с целью уменьшения частоты назначений антибиотиков по этому показанию.
5. Выводы
Приведенные выше данные из реальной практики указывают на то, что Канефрон® является эффективным и безопасным средством симптоматической терапии острого цистита или ИСШ. В долгосрочной перспективе показатели частоты дополнительного назначения антибиотиков и рецидивов ИСШ после лечения Канефроном были даже значительно ниже, чем после лечения антибиотиками. Таким образом, препарат Канефрон следует рассматривать в качестве альтернативного средства лечения; в частности, учитывая необходимость более широкого внедрения стратегии рационального использования противомикробных препаратов.
Личный вклад авторов: Автор K.K. занимался разработкой дизайна исследования, провел статистический анализ, занимался литературным поиском, написал первый черновой вариант рукописи и занимался корректурой рукописи. Авторы M.H., H.S., D.A.-S., F.W., K.G.N. занимались разработкой дизайна исследования, литературным поиском и корректурой рукописи. Все авторы прочли опубликованную версию рукописи и согласовали ее.
Финансирование: Проведение этого исследования финансировалось компанией «Бионорика СЭ» (г. Ноймаркт, Германия).
Заявление по этическим аспектам проведения исследования: Законодательство Германии при определенных условиях разрешает использование в исследовательских целях анонимных данных электронной медицинской документации. Согласно этому законодательству, для проведения такого типа обсервационного исследования, не предусматривающего использование данных, которые могли бы непосредственно идентифицировать пациента, нет необходимости получать информированное согласие от пациентов или разрешение соответствующего экспертного совета учреждения здравоохранения (ЭРЖ). Поскольку данные о пациентах спрашивали только в совокупном виде и в ответ на такие запросы не предоставлялось никакой конфиденциальной медицинской информации, для использования этой базы данных и для проведения данного исследования не требовалось никаких разрешений от ЭРЖ.
Заявление о предоставлении информированного согласия: Н/З.
Заявление о наличии данных: Данные, представленные в данном исследовании, доступны по запросу соответствующего автора.
Конфликт интересов: Авторы Martina Höller, Hubert Steindl, Dimitri Abramov-Sommariva являются штатными работниками компании «Бионорика СЕ»; автор Karel Kostev является штатным сотрудником компании IQVIA и не декларирует никаких других конфликтов интересов. Автор Kurt G. Naber сообщает о получении персонального вознаграждения от компании «Бионорика», а также о получении персонального вознаграждения от компании «Adamed», персонального вознаграждения от компании «Allecra», персонального вознаграждения от компании «Apogepha», персонального вознаграждения от компании «Enteris Biopharma», персональное вознаграждение от компании «Galenus», персональное вознаграждение от компании «GlaxoSmithKline», персональное вознаграждение от компании «Hermes», персональное вознаграждение от компании «Leo», персональное вознаграждение от компании «Medice», персональное вознаграждение от компании «MerLion» , персональное вознаграждение от компании «MSD SHARP& DOHME», персональное вознаграждение от компании «Paratek», персональное вознаграждение от компании «Roche», персональное вознаграждение от компании «Rosen», персональное вознаграждение от компании «Saxonia» и персональное вознаграждение от компании «Vifor» , что не касается данной работы. FW сообщает о получении персонального вознаграждения от компании «Бионорика», а также о получении персонального вознаграждения и других средств от компании «Achaogen», персонального вознаграждения от компании «AstraZeneca», других средств от компании «Enteris BioPharma», других средств от компании «Helperby Therapeutics Ltd.», персональное вознаграждение от компании «Janssen», персональное вознаграждение от компании «LeoPharma», персональное вознаграждение от компании «MerLion», персональное вознаграждение от компании «MSD», персональное вознаграждение от компаний «OM Pharma/Vifor Pharma», персональное вознаграждение от компании «OMPharma/Vifor Pharma» вознаграждения от компании «Pfizer», персонального вознаграждения от компании «RosenPharma», персонального вознаграждения и других средств от компании «Shionogi», персонального вознаграждения от компании «VenatoRx» и персонального вознаграждения от компании «GSK», не касающегося данной работы.
Список литературы
Flores-Mireles, A.L.; Walker, J.N.; Caparon, M.; Hultgren, S.J. Urinary tract infections: Epidemiology, mechanisms of infection and treatment options. Nat. Rev. Microbiol. 2015, 13, 269‒284. [CrossRef] [PubMed]
Schmiemann, G.; Kniehl, E.; Gebhardt, K.; Matejczyk, M.M.; Hummers, E. The Diagnosis of Urinary Tract Infection. Dtsch. Aerzteblatt Online 2010, 107, 361‒367. [CrossRef] [PubMed]
Foxman, B. Epidemiology of urinary tract infections: Incidence, morbidity, and economic costs. Am. J. Med. 2002, 113, 5‒13. [CrossRef]
Colgan, R.; Williams, M. Diagnosis and treatment of acute uncomplicated cystitis. Am. Fam. Physician 2011, 84, 771‒776.
Bonkat, G.; Bartoletti, R.; Bruyère, F.; Cai, T.; Geerlings, S.E.; Köves, B.; Schubert, S.; Wagenlehner, F.; Mezei, T.; Pilatz, A.; et al. European Association of Urology Guidelines on Urological Infections; EAU Guidelines Office: Arnhem, The Netherlands, 2020; ISBN 978-94-92671-07-3. Available online: https://uroweb.org/guideline/urological-infections/ (accessed on 4 January 2021).
Kranz, J.; Schmidt, S.; Lebert, C.; Schneidewind, L.; Mandraka, F.; Kunze, M.; Helbig, S.; Vahlensieck, W.; Naber, K.; Schmiemann, G.; et al. The 2017 Update of the German Clinical Guideline on Epidemiology, Diagnostics, Therapy, Prevention, and Management of Uncomplicated Urinary Tract Infections in Adult Patients. Part II: Therapy and Prevention. Urol. Int. 2018, 100, 271‒278. [CrossRef]
Christiaens, T.C.M.; De Meyere, M.; Verschraegen, G.; Peersman, W.; Heytens, S.; De Maeseneer, J.M. Randomised controlled trial of nitrofurantoin versus placebo in the treatment of uncomplicated urinary tract infection in adult women. Br. J. Gen. Pract. 2002, 52, 729‒734. [PubMed]
Gagyor, I.; Bleidorn, J.; Kochen, M.M.; Schmiemann, G.; Wegscheider, K.; Hummers-Pradier, E. Ibuprofen versus fosfomycin for uncomplicated urinary tract infection in women: Randomised controlled trial. BMJ 2015, 351, h6544. [CrossRef] [PubMed]
Bleidorn, J.; Hummers-Pradier, E.; Schmiemann, G.; Wiese, B.; Gágyor, I. Recurrent urinary tract infections and complications after symptomatic versus antibiotic treatment: Follow-up of a randomised controlled trial. Ger. Med. Sci. 2016, 14. [CrossRef]
Kronenberg, A.; Bütikofer, L.; Odutayo, A.; Mühlemann, K.; Da Costa, B.R.; Battaglia, M.; Meli, D.N.; Frey, P.; Limacher, A.; Reichenbach, S.; et al. Symptomatic treatment of uncomplicated lower urinary tract infections in the ambulatory setting: Randomised, double blind trial. BMJ 2017, 359, j4784. [CrossRef]
Stange, R.; Schneider, B.; Albrecht, U.; Mueller, V.; Schnitker, J.; Michalsen, A. Results of a randomized, prospective, double-dummy, double-blind trial to compare efficacy and safety of a herbal combination containing Tropaeoli majoris herba and Armoraciae rusticanae radix with co-trimoxazole in patients with acute and uncomplicated cystitis. Res. Rep. Urol. 2017, 9, 43‒50. [CrossRef]
Wawrysiuk, S.; Naber, K.; Rechberger, T.; Miotla, P. Prevention and treatment of uncomplicated lower urinary tract infections in the era of increasing antimicrobial resistance—non-antibiotic approaches: A systemic review. Arch. Gynecol. Obstet. 2019, 300, 821‒828. [CrossRef] [PubMed]
Naber, K.G. Efficacy and safety of the phytotherapeutic drug Canephron® N in prevention and treatment of urogenital and gestational disease: Review of clinical experience in Eastern Europe and Central Asia. Res. Rep. Urol. 2013, 5, 39‒46. [CrossRef]
Brenneis, C.; Künstle, G.; Haunschild, J. Spasmolytic activity of Canephron N on the contractility of rat and human isolated urinary bladder. In Proceedings of the 13th Congress of the International Society for Ethnopharmacology, Graz, Austria, 2‒6 September 2012.
Haloui, M.; Louedec, L.; Michel, J.-B.; Lyoussi, B. Experimental diuretic effects of Rosmarinus officinalis and Centaurium erythraea. J. Ethnopharmacol. 2000, 71, 465‒472. [CrossRef]
Nausch, B.; Künstle, G.; Mönch, B.; Koeberle, A.; Werz, O.; Haunschild, J. Canephron® N alleviates pain in experimental cystitis and inhibits reactive oxygen/nitrogen species as well as microsomal prostaglandin E2 synthase-1. Der Urol. 2015, 54, 28.
Künstle, G.; Brenneis, C.; Haunschild, J. 671 Efficacy of Canephron® N against bacterial adhesion, inflammation and bladder hyperactivity. Eur. Urol. Suppl. 2013, 12, e671. [CrossRef]
Nausch, B.; Pace, S.; Pein, H.; Koeberle, A.; Rossi, A.; Künstle, G.; Werz, O. The standardized herbal combination BNO 2103 contained in Canephron® N alleviates inflammatory pain in experimental cystitis and prostatitis. Phytomedicine 2019, 60, 152987. [CrossRef]
Davidov, M.I.; Bunova, N.E. Comparative assessment of Canephron® N and ciprofloxacin as monotherapy of acute uncomplicated cystitis in women. Urologiia 2018, 4, 24‒32. [CrossRef]
Davidov, M.I.; Voitko, D.A.; Bunova, N.E. Treatment of acute uncomplicated cystitis in women with antibiotic allergy or intolerance. Urologiia 2019, 5, 64‒71. [CrossRef]
Wagenlehner, F.M.; Abramov-Sommariva, D.; Höller, M.; Steindl, H.; Naber, K.G. Non-Antibiotic Herbal Therapy (BNO 1045) versus Antibiotic Therapy (Fosfomycin Trometamol) for the Treatment of Acute Lower Uncomplicated Urinary Tract Infections in Women: A Double-Blind, Parallel-Group, Randomized, Multicentre, Non-Inferiority Phase III Trial. Urol. Int. 2018, 101, 327‒336. [CrossRef]
Haynes, B. Can it work? Does it work? Is it worth it? The testing of healthcare interventions is evolving. BMJ 1999, 319, 652‒653. [CrossRef] [PubMed]
Rathmann, W.; Bongaerts, B.; Carius, H.-J.; Kruppert, S.; Kostev, K. Basic characteristics and representativeness of the German Disease Analyzer database. Int. J. Clin. Pharmacol. Ther. 2018, 56, 459‒466. [CrossRef]
Quan, H.; Sundararajan, V.; Halfon, P.; Fong, A.; Burnand, B.; Luthi, J.C.; Saunders, L.D.; Beck, C.A.; Feasby, T.E.; Ghali, W.A. Coding algorithms for defining comorbidities in ICD-9-CM and ICD-10 administrative data. Med. Care 2005, 43, 1130‒1139. [CrossRef]
Amdii, R.E.; Al-Shukri, S.K.; Kuzmin, I.V.; Sorokin, N.V.; Chaplitskiy, E.A.; Skvortsov, M.V.; Alekseev, A.S.; Okunchaev, A.S.; Turbin, A.A.; Timaeva, G.R.; et al. Use of Canephron N in treatment of acute uncomplicated cystitis in women. Urologicheskie Vedomosti 2016, 6, 16‒22. [CrossRef]
Sabadash, M.; Shulyak, A. Canephron® N in the treatment of recurrent cystitis in women of child-bearing Age: A randomised controlled study. Clin. Phytoscience 2017, 3, 9. [CrossRef]
Serov, V.N.; Baranov, I.I.; Protopopova, N.V.; Tkachenko, L.V.; Kukarskaya, I.I. Evaluation of experience with a combination phytotherapeutic drug in pregnant women (a multicenter retrospective observational study). Obstet. Gynecol. 2013, 9, 105‒112.
Dudar, I.O.; Loboda, O.M.; Krot, V.F.; Khimich, V.I.; Kryzhanivska, V.M.; Bryzhachenko, T.P. A 12-month comparative study of Canephron® N administration in the treatment of patients with the urinary tract infection. Zdorovie Muzhchiny 2010, 3, 85‒90.
Ordzhonikidze, N.V.; Yemelyanova, A.I.; Petrova, S.B. Complication prevention and treatment in pregnants and puerperants with urinary tract diseases. Obstet. Gynaecol. 2009, 6, 41‒45.
Perepanova, T.S.; Khazan, P.L. Phytopreparation Canephron® N in the treatment and prophylaxis of urinary tract infections. Vrachebnoye Soslovie 2005, 5, 44‒46.
Ivanov, D.; Abramov-Sommariva, D.; Moritz, K.; Eskötter, H.; Kostinenko, T.; Martynyuk, L.; Kolesnik, N.; Naber, K.G. An open label, non-controlled, multicentre, interventional trial to investigate the safety and efficacy of Canephron® N in the management of uncomplicated urinary tract infections (uUTIs). Clin. Phytoscience 2015, 1, 7. [CrossRef]
Naber, K.G.; Kogan, M.; Wagenlehner, F.M.E.; Siener, R.; Gessner, A. How the microbiome is influenced by the therapy of urological diseases: Standard versus alternative approaches. Clin. Phytoscience 2017, 3, 8. [CrossRef]
Cai, T.; Verze, P.; Palmieri, A.; Gacci, M.; Lanzafame, P.; Malossini, G.; Nesi, G.; Bonkat, G.; Wagenlehner, F.M.; Mirone, V.; et al. Is Preoperative Assessment and Treatment of Asymptomatic Bacteriuria Necessary for Reducing the Risk of Postoperative Symptomatic Urinary Tract Infections After Urologic Surgical Procedures? Urology 2017, 99, 100‒105. [CrossRef]
Wullt, B.; Svanborg, C. Deliberate Establishment of Asymptomatic Bacteriuria—A Novel Strategy to Prevent Recurrent UTI. Pathogens 2016, 5, 52. [CrossRef]
Martin, D.; Konrad, M.; Adarkwah, C.C.; Kostev, K. Reduced antibiotic use after initial treatment of acute respiratory infections with phytopharmaceuticals- a retrospective cohort study. Postgrad. Med. 2020, 132, 412‒418. [CrossRef] [PubMed]
